Sự phục hồi chức năng bàng quang sau phẫu thuật giải tắc đường ra bàng quang do bệnh lý tuyến tiền liệt: Cơ chế sinh lý bệnh, tiến trình phục hồi và yếu tố tiên lượng.
Tóm tắt
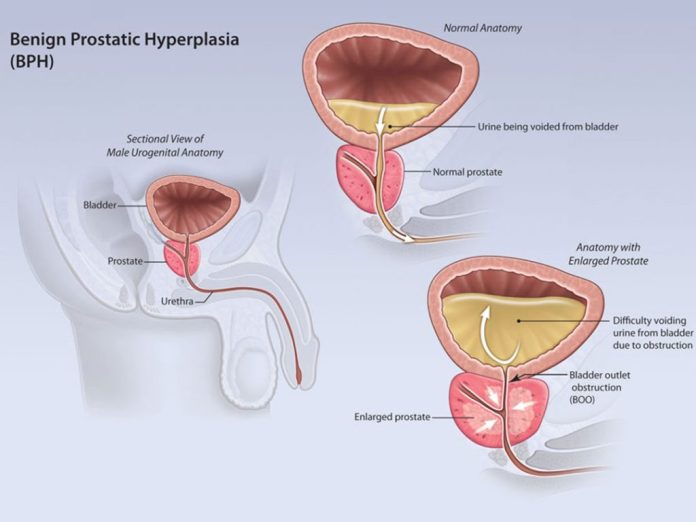
Tắc nghẽn đường ra bàng quang (Bladder Outlet Obstruction – BOO) do tăng sinh lành tính tuyến tiền liệt (Benign Prostatic Hyperplasia – BPH) là một trong những bệnh lý niệu khoa phổ biến nhất ở nam giới cao tuổi, gây ra những biến đổi sâu sắc về cấu trúc và chức năng của đường tiết niệu dưới. Mặc dù các can thiệp ngoại khoa giải áp như cắt đốt nội soi qua niệu đạo (TURP), bóc nhân bằng laser (HoLEP, ThuLEP) hay bốc hơi quang chọn lọc (PVP) đã đạt được những tiến bộ vượt bậc trong việc giải quyết tắc nghẽn cơ học, sự phục hồi chức năng của bàng quang sau phẫu thuật vẫn là một vấn đề phức tạp và chưa được hiểu biết thấu đáo. Tình trạng rối loạn chức năng bàng quang tồn dư—bao gồm bàng quang tăng hoạt (OAB), giảm hoạt cơ chóp (Detrusor Underactivity – DU), và giảm độ giãn nở (compliance)—tiếp tục ảnh hưởng đến chất lượng cuộc sống của một tỷ lệ đáng kể bệnh nhân sau can thiệp.
Báo cáo nghiên cứu này cung cấp một phân tích toàn diện, đa chiều về quá trình phục hồi chức năng bàng quang sau phẫu thuật giải tắc nghẽn, dựa trên việc tổng hợp các dữ liệu lâm sàng và thực nghiệm mới nhất. Phân tích đi sâu vào ba trụ cột chính: (1) Cơ chế sinh lý bệnh học phân tử, tập trung vào vai trò của stress oxy hóa, tổn thương thiếu máu cục bộ-tái tưới máu (I/R), và các con đường tín hiệu xơ hóa như TGF-beta/HIF-1alpha trong quá trình tái cấu trúc thành bàng quang; (2) Tiến trình phục hồi chức năng, đánh giá động học của các thông số niệu động học và triệu chứng lâm sàng theo thời gian, cũng như so sánh hiệu quả giữa các phương thức phẫu thuật khác nhau; và (3) Các yếu tố tiên lượng, xác định những chỉ số lâm sàng và cận lâm sàng giúp dự đoán khả năng hồi phục, từ đó tối ưu hóa chiến lược quản lý hậu phẫu. Báo cáo cũng thảo luận về các hướng đi tương lai trong y học tái tạo và liệu pháp hỗ trợ nhằm cải thiện kết quả điều trị cho nhóm bệnh nhân có bàng quang mất bù.
1. Cơ sở Sinh lý bệnh của Tái cấu trúc Bàng quang do Tắc nghẽn
Sự hiểu biết sâu sắc về cơ chế sinh lý bệnh ở cấp độ tế bào và phân tử là chìa khóa để giải thích tại sao sự phục hồi chức năng bàng quang không phải lúc nào cũng song hành với việc giải quyết tắc nghẽn cơ học. Quá trình tái cấu trúc bàng quang (bladder remodeling) là một phản ứng thích nghi phức tạp trước sự gia tăng sức cản đường ra, diễn ra qua nhiều giai đoạn và chịu sự chi phối của nhiều con đường tín hiệu.
1.1. Mô hình Ba Giai đoạn của Tái cấu trúc Bàng quang
Dựa trên các nghiên cứu mô bệnh học và niệu động học trên cả mô hình động vật và con người, quá trình đáp ứng của bàng quang đối với tắc nghẽn đường ra được chia thành ba giai đoạn liên tiếp, phản ánh cuộc chiến giữa cơ chế bù trừ và sự suy sụp chức năng.
1.1.1. Giai đoạn Phì đại và Tăng hoạt (Hypertrophy Phase)
Trong giai đoạn đầu của tắc nghẽn, bàng quang phải tạo ra áp lực cao hơn để thắng sức cản niệu đạo và tống xuất nước tiểu. Đáp ứng sinh lý tức thì là sự phì đại của lớp cơ trơn bàng quang (detrusor smooth muscle).
- Cơ chế tế bào: Các tế bào cơ trơn (SMCs) trải qua quá trình phì đại (tăng kích thước) hơn là tăng sản (tăng số lượng). Sự căng giãn cơ học chu kỳ (cyclic stretch) trong quá trình chứa đựng và áp lực thủy tĩnh cao trong quá trình đi tiểu là những kích thích vật lý chính kích hoạt các thụ thể màng tế bào.
- Tín hiệu phân tử: Con đường tín hiệu Calcineurin-NFAT đóng vai trò trung tâm. Sự gia tăng nồng độ Canxi nội bào do căng giãn cơ học kích hoạt Calcineurin, một phosphatase phụ thuộc canxi. Calcineurin khử phosphoryl hóa yếu tố nhân của tế bào T hoạt hóa (NFAT), cho phép nó di chuyển vào nhân và kích hoạt phiên mã các gen gây phì đại cơ.
- Biểu hiện lâm sàng: Bàng quang trong giai đoạn này thường biểu hiện tình trạng tăng hoạt (Detrusor Overactivity – DO). Sự phì đại làm thay đổi tính hưng phấn điện học của màng tế bào, tăng cường kết nối khe (gap junctions) giữa các tế bào cơ, dẫn đến các co thắt không tự chủ, biểu hiện bằng triệu chứng tiểu gấp và tiểu nhiều lần.
1.1.2. Giai đoạn Bù trừ (Compensation Phase)
Nếu tắc nghẽn tiếp diễn, bàng quang bước vào giai đoạn bù trừ ổn định.
- Cân bằng mong manh: Khối lượng cơ bàng quang tăng lên đáng kể, cho phép duy trì áp lực tống xuất và làm rỗng bàng quang tương đối hiệu quả. Tuy nhiên, tốc độ dòng chảy tối đa (Qmax) bắt đầu giảm và thời gian đi tiểu kéo dài.
- Thay đổi chuyển hóa: Mặc dù chức năng tống xuất được duy trì, nhưng sự phì đại quá mức bắt đầu vượt quá khả năng cung cấp oxy và dinh dưỡng của hệ thống vi mạch. Các tế bào cơ chuyển sang chuyển hóa kỵ khí, dẫn đến tích tụ acid lactic và giảm dự trữ năng lượng, đặt nền móng cho tổn thương tế bào.
1.1.3. Giai đoạn Mất bù (Decompensation Phase)
Đây là giai đoạn cuối cùng và nguy hiểm nhất, đặc trưng bởi sự suy giảm khả năng co bóp và giãn nở của bàng quang.
- Thoái hóa và Xơ hóa: Các tế bào cơ trơn bị tổn thương không hồi phục và trải qua quá trình chết theo chương trình (apoptosis) hoặc hoại tử. Không gian gian bào bị lấp đầy bởi sự lắng đọng quá mức của collagen và chất nền ngoại bào (ECM), dẫn đến xơ hóa thành bàng quang.
- Rối loạn chức năng: Bàng quang trở nên xơ cứng, giảm độ đàn hồi (low compliance), gây tăng áp lực chứa đựng nguy hiểm cho thận. Đồng thời, khả năng co bóp suy giảm dẫn đến bàng quang giảm hoạt (DU) hoặc mất trương lực, gây bí tiểu mạn tính và tồn dư nước tiểu lớn.
1.2. Vai trò Trung tâm của Stress Oxy hóa và Tổn thương Thiếu máu cục bộ – Tái tưới máu (I/R)
Một trong những cơ chế bệnh sinh quan trọng nhất dẫn đến rối loạn chức năng bàng quang trong BOO là tổn thương do thiếu máu cục bộ và tái tưới máu (Ischemia/Reperfusion Injury).
- Cơ chế Huyết động học: Khi bàng quang căng đầy hoặc co bóp mạnh để thắng tắc nghẽn, áp lực nội bàng quang tăng cao nén ép các mạch máu nuôi dưỡng trong thành bàng quang, gây ra thiếu máu cục bộ. Khi bàng quang được làm rỗng (sau khi tiểu hoặc sau phẫu thuật), máu dồn trở lại ồ ạt gây ra tổn thương tái tưới máu.
- Sản sinh Gốc Tự do (ROS): Quá trình tái tưới máu kích hoạt sự sản sinh ồ ạt các loại oxy phản ứng (Reactive Oxygen Species – ROS) như superoxide anion và peroxynitrite. Nghiên cứu trên mô hình thỏ bị tắc nghẽn một phần (PBOO) cho thấy sự gia tăng đáng kể các chất chỉ thị stress oxy hóa như 8-hydroxy-2′-deoxyguanosine (8-OHdG) trong nước tiểu và mô, cùng với malondialdehyde (MDA) trong huyết tương.
- Tổn thương Ty thể: ROS tấn công trực tiếp vào ty thể, nơi sản xuất năng lượng cho tế bào cơ. Sự giảm số lượng bản sao DNA ty thể và tổn thương màng ty thể làm suy giảm nghiêm trọng khả năng tổng hợp ATP, khiến cơ bàng quang yếu đi và dễ bị mệt mỏi, góp phần trực tiếp vào bệnh sinh của bàng quang giảm hoạt (DU).
1.3. Con đường Tín hiệu Xơ hóa và Viêm: TGF-beta và HIF-1alpha
Sự chuyển đổi từ phì đại sang xơ hóa được điều phối bởi một mạng lưới phức tạp các cytokine và yếu tố tăng trưởng.
- Trục Hypoxia – HIF-1alpha: Thiếu oxy mạn tính kích hoạt yếu tố cảm ứng thiếu oxy 1-alpha (HIF-1alpha). Sự biểu hiện quá mức của HIF-1alpha trong tế bào biểu mô bàng quang thúc đẩy quá trình chuyển dạng biểu mô-trung mô (Epithelial-Mesenchymal Transition – EMT) và pyroptosis (chết tế bào dạng viêm), là nguồn gốc quan trọng của nguyên bào sợi gây xơ hóa.
- Trục TGF-beta: Yếu tố tăng trưởng chuyển dạng beta (TGF-beta) là chất trung gian mạnh nhất của quá trình xơ hóa. Tắc nghẽn làm tăng nồng độ TGF-beta, kích thích nguyên bào sợi tăng sinh và sản xuất collagen type I và III, làm dày thành bàng quang và giảm độ giãn nở. Các nghiên cứu cho thấy ức chế con đường TGF-beta có thể làm giảm xơ hóa thận và gan, gợi ý tiềm năng tương tự trên bàng quang.
- Phản ứng Viêm: Stress oxy hóa và hoại tử tế bào kích hoạt hệ thống miễn dịch bẩm sinh. Sự xâm nhập của đại thực bào và bạch cầu trung tính, cùng với việc giải phóng các cytokine tiền viêm (IL-1beta, IL-6, TNF-alpha) và kích hoạt phức hợp NLRP3 inflammasome, tạo ra một vòng xoắn bệnh lý duy trì quá trình viêm và xơ hóa ngay cả khi tắc nghẽn đã được giải quyết.
1.4. Biến đổi Thần kinh (Neuroplasticity)
Hệ thần kinh chi phối bàng quang cũng chịu những tổn thương sâu sắc do BOO.
- Mất phân bố thần kinh (Denervation): Tắc nghẽn kéo dài và thiếu máu cục bộ dẫn đến thoái hóa các sợi thần kinh trục (axonal degeneration) và giảm mật độ thần kinh trong cơ chóp.
- Quá mẫn cảm (Supersensitivity): Mặc dù số lượng dây thần kinh giảm, các thụ thể hậu synap (đặc biệt là thụ thể muscarinic M2, M3 và purinergic P2X) trở nên quá mẫn cảm với chất dẫn truyền thần kinh (Acetylcholine, ATP). Điều này giải thích nghịch lý tại sao bàng quang vừa có sức co bóp yếu (do mất thần kinh và tổn thương cơ) lại vừa có biểu hiện tăng hoạt (do quá mẫn thụ thể).
2. Các Phương pháp Phẫu thuật và Tác động lên Sự Phục hồi
Sự lựa chọn phương pháp phẫu thuật đóng vai trò quan trọng, không chỉ trong việc giải quyết tắc nghẽn cơ học mà còn ảnh hưởng đến môi trường phục hồi của bàng quang thông qua mức độ xâm lấn, khả năng bảo tồn mô và phản ứng viêm hậu phẫu.
2.1. Cắt đốt nội soi qua niệu đạo (TURP) – Tiêu chuẩn vàng
TURP (Transurethral Resection of the Prostate) đơn cực hoặc lưỡng cực vẫn là tiêu chuẩn vàng trong điều trị ngoại khoa BPH, đặc biệt cho các tuyến có kích thước trung bình (30-80ml).
- Cơ chế: Sử dụng dòng điện để cắt nhỏ mô tuyến thành từng mảnh (chips).
- Tác động phục hồi: TURP mang lại sự cải thiện ổn định và lâu dài về Qmax và IPSS. Các nghiên cứu theo dõi dài hạn (lên đến 20 năm) cho thấy sự cải thiện triệu chứng bền vững, mặc dù có tỷ lệ tái can thiệp khoảng 10-15% sau 10-15 năm do mô tuyến mọc lại hoặc xơ hẹp cổ bàng quang/niệu đạo.
- Hạn chế: TURP để lại một bề mặt vết thương rộng trong niệu đạo tuyến tiền liệt, cần thời gian để biểu mô hóa lại (4-6 tuần). Quá trình viêm và bong vảy trong giai đoạn này có thể gây ra các triệu chứng kích thích kéo dài.

2.2. Bóc nhân Tuyến tiền liệt bằng Laser (HoLEP và ThuLEP)
Các kỹ thuật bóc nhân (Enucleation) sử dụng laser Holmium (HoLEP) hoặc Thulium (ThuLEP) đang ngày càng thay thế TURP và mổ mở, đặc biệt cho các tuyến kích thước lớn (>80-100g).
- Cơ chế: Mô phỏng kỹ thuật mổ mở bằng cách bóc tách trọn vẹn thùy tuyến (adenoma) ra khỏi vỏ bao (surgical capsule) bằng năng lượng laser, sau đó xay nhỏ mô (morcellation) để lấy ra ngoài.
- Ưu điểm phục hồi:
- Giải áp triệt để: Bóc nhân loại bỏ hoàn toàn mô tuyến, đưa thể tích tuyến về mức bình thường (giống như sau mổ mở), giúp giảm tối đa sức cản đường ra. Điều này tạo điều kiện huyết động học tốt nhất cho bàng quang phục hồi, dẫn đến chỉ số Qmax và giảm PVR thường vượt trội hơn so với TURP ở các tuyến lớn.
- Giảm tổn thương nhiệt: Laser Thulium (ThuLEP) có độ xuyên sâu nông (0.2mm) so với Holmium (0.4mm) và dao điện, giúp giảm thiểu tổn thương nhiệt lên các cấu trúc lân cận (thần kinh cương, cơ thắt ngoài), từ đó giảm phản ứng viêm và kích thích bàng quang sau mổ.
- Rút ngắn thời gian hồi phục: Thời gian lưu thông tiểu ngắn hơn (thường <24h) so với TURP giúp bệnh nhân sớm tập lại phản xạ đi tiểu tự nhiên.

2.3. Bốc hơi quang chọn lọc (GreenLight PVP)
- Cơ chế: Sử dụng laser bước sóng 532nm (màu xanh lá) để làm bốc hơi mô tuyến và cầm máu quang học.
- Tác động phục hồi: PVP rất hiệu quả trong việc cầm máu, phù hợp cho bệnh nhân đang dùng thuốc chống đông. Tuy nhiên, PVP tạo ra một lớp mô hoại tử đông (coagulation necrosis) dày hơn so với cắt đốt hoặc bóc nhân. Lớp mô này cần thời gian để bong tróc và đào thải, thường gây ra các triệu chứng kích thích (tiểu buốt, tiểu gấp, tiểu nhiều lần) kéo dài hơn trong 1-3 tháng đầu sau phẫu thuật, làm chậm quá trình cảm nhận sự phục hồi chủ quan của bệnh nhân. Dữ liệu dài hạn 12 năm cho thấy kết quả bền vững nhưng tỷ lệ tái can thiệp có thể cao hơn HoLEP do mô tuyến mọc lại nếu không bốc hơi triệt để.
2.4. Phẫu thuật Robot hỗ trợ (RASP)
- Chỉ định: Dành cho các tuyến tiền liệt rất lớn (>100-150g).
- So sánh với HoLEP: Các phân tích gộp (meta-analysis) cho thấy RASP và HoLEP mang lại kết quả chức năng (IPSS, Qmax) tương đương nhau. Tuy nhiên, HoLEP vượt trội hơn về tính xâm lấn tối thiểu, thời gian nằm viện ngắn hơn, thời gian lưu thông tiểu ngắn hơn và ít mất máu hơn. RASP có ưu thế về đường cong học tập ngắn hơn cho phẫu thuật viên.
3. Tiến trình Phục hồi Chức năng Bàng quang theo Thời gian
Sự phục hồi sau phẫu thuật không phải là một sự kiện tức thời mà là một quá trình động học diễn ra qua nhiều tháng, thậm chí nhiều năm. Các thông số khác nhau của chức năng bàng quang hồi phục với tốc độ khác nhau.
3.1. Phục hồi Dòng chảy và Làm rỗng (Qmax và PVR)
Đây là những thông số cải thiện nhanh chóng và ngoạn mục nhất.
- Ngay sau phẫu thuật (0-1 tháng): Ngay sau khi rút thông tiểu, sức cản niệu đạo giảm đột ngột. Qmax thường tăng gấp đôi (từ trung bình 8-10 ml/s lên 15-20 ml/s). Tồn dư nước tiểu (PVR) giảm mạnh, thường giảm >60-70% so với trước mổ.
- Ổn định: Các chỉ số này thường đạt đỉnh và ổn định sau 3-6 tháng. Sự tồn tại của PVR cao (>150ml) sau giai đoạn này là dấu hiệu cảnh báo của bàng quang giảm hoạt (DU) không hồi phục hoặc tắc nghẽn tồn dư/thứ phát (như xơ hẹp niệu đạo).
3.2. Phục hồi Áp lực Cơ chóp và Sức co bóp
- Hiện tượng giảm áp lực: Một hiện tượng thú vị quan sát được trên niệu động học là áp lực cơ chóp tại dòng chảy tối đa (Pdet@Qmax) giảm đi đáng kể sau phẫu thuật. Điều này không phản ánh sự suy yếu của cơ, mà là sự thích nghi sinh lý: bàng quang không còn cần phải tạo ra áp lực cực lớn để thắng sức cản đường ra.
- Hồi phục sức co bóp: Đối với những bệnh nhân có bàng quang giảm hoạt (DU) trước mổ (BCI < 100), câu hỏi về khả năng hồi phục vẫn còn tranh cãi. Một số nghiên cứu cho thấy việc giải áp có thể cải thiện một phần sức co bóp nếu tổn thương chưa đến mức xơ hóa hoàn toàn. Tuy nhiên, nhiều bệnh nhân DU vẫn tiếp tục có dòng chảy yếu dù không còn tắc nghẽn, do tổn thương cơ và thần kinh là không thể đảo ngược.
3.3. Phục hồi Độ giãn nở (Compliance) và Triệu chứng Chứa đựng
Sự phục hồi chức năng chứa đựng thường chậm trễ hơn nhiều so với chức năng tống xuất.
- Giai đoạn sớm (1-3 tháng): Tình trạng tiểu gấp, tiểu nhiều lần, tiểu đêm có thể không cải thiện ngay, thậm chí tồi tệ hơn tạm thời do phản ứng viêm tại chỗ, phù nề niệu đạo hoặc sự mất ổn định của cơ chóp sau giải áp. Khoảng 20-30% bệnh nhân vẫn còn triệu chứng OAB trong giai đoạn này.
- Giai đoạn muộn (6-12 tháng): Độ giãn nở bàng quang (Compliance) cải thiện dần dần khi quá trình viêm thoái lui và một phần xơ hóa được tái cấu trúc. Nghiên cứu cho thấy độ giãn nở trung bình có thể tăng từ 3.06 ml/cmH2O lên 13.53 ml/cmH2O. Tuy nhiên, ở những bệnh nhân có bàng quang nhỏ, xơ cứng lâu ngày (low compliance bladder), sự phục hồi dung tích thường hạn chế và nguy cơ suy thận tiềm ẩn vẫn còn.
3.4. Khả năng Đảo ngược (Reversibility) ở cấp độ Phân tử
Dữ liệu thực nghiệm cho thấy việc giải áp kịp thời có thể đảo ngược các tổn thương phân tử. Mức độ các chất đánh dấu stress oxy hóa (MDA, 8-OHdG) và các yếu tố gây xơ hóa (TGF-beta) giảm dần về mức bình thường sau khi giải tắc nghẽn. Tuy nhiên, “cửa sổ cơ hội” là hữu hạn; nếu can thiệp quá muộn khi ty thể đã bị phá hủy và collagen đã thay thế hoàn toàn mô cơ, sự phục hồi là bất khả thi.
4. Các Yếu tố Tiên lượng Phục hồi Chức năng
Khả năng dự đoán kết quả chức năng trước phẫu thuật là vô cùng quan trọng để tư vấn cho bệnh nhân và thiết lập kỳ vọng thực tế.
4.1. Yếu tố Lâm sàng và Nhân trắc học
| Yếu tố | Tác động Tiên lượng | Giải thích Cơ chế & Bằng chứng |
| Tuổi tác | Tiên lượng nghịch | Bệnh nhân cao tuổi (>70-80) có khả năng phục hồi kém hơn về chức năng co bóp và kiểm soát tiểu tiện. Lão hóa tự nhiên làm giảm mật độ thần kinh và dự trữ năng lượng tế bào cơ. |
| Thời gian mắc bệnh | Tiên lượng nghịch | Thời gian tắc nghẽn càng dài, nguy cơ xơ hóa không hồi phục càng cao. Một nghiên cứu xác định ngưỡng thời gian >16 tháng là yếu tố tiên lượng xấu cho kết quả TURP. |
| Bệnh đồng mắc | Tiên lượng nghịch | Đái tháo đường, bệnh mạch máu gây cộng hưởng tổn thương vi mạch và thần kinh, làm giảm khả năng phục hồi sau giải áp. |
| Độ dài niệu đạo màng | Tiên lượng thuận (cho tự chủ) | Độ dài niệu đạo màng (MUL) đo trên MRI trước mổ >14-15mm dự báo khả năng phục hồi tự chủ tiểu tiện sớm và hoàn toàn tốt hơn sau phẫu thuật. |
4.2. Yếu tố Cận lâm sàng và Hình ảnh học
4.2.1. Độ dày thành bàng quang (Bladder Wall Thickness – BWT/DWT)
Đo độ dày cơ chóp (DWT) qua siêu âm là một công cụ tiên lượng không xâm lấn đầy tiềm năng.
- Ý nghĩa: DWT tăng (>2mm) phản ánh tình trạng phì đại do tắc nghẽn.
- Tiên lượng: Sau phẫu thuật thành công, DWT giảm đáng kể, tương quan với sự cải thiện triệu chứng. Nếu DWT không giảm sau mổ, điều này gợi ý tắc nghẽn tồn dư hoặc phản ứng viêm/xơ hóa mạn tính. Nhóm bệnh nhân có DWT dày trước mổ thường có kết quả giải áp tốt hơn (do tắc nghẽn là nguyên nhân chính), trong khi nhóm có DWT mỏng kèm LUTS nặng thường gợi ý bàng quang giảm hoạt nguyên phát hoặc lão hóa, ít đáp ứng với phẫu thuật hơn.
4.2.2. Các Chỉ số Niệu động học (Urodynamic Indices)
- Chỉ số Tắc nghẽn (BOOI): BOOI > 40 (tắc nghẽn rõ) là yếu tố dự báo mạnh mẽ cho sự thành công của phẫu thuật. Bệnh nhân có BOOI < 20 (không tắc nghẽn) hoặc vùng xám (20-40) thường có tỷ lệ cải thiện triệu chứng thấp hơn sau mổ.
- Chỉ số Co bóp (BCI): BCI < 100 (Bàng quang giảm hoạt – DU) là một thách thức. Tuy nhiên, các nghiên cứu gần đây chỉ ra rằng bệnh nhân DU kèm theo tắc nghẽn (BOO+DU) vẫn có thể hưởng lợi từ phẫu thuật (giảm PVR, cải thiện dòng chảy), mặc dù mức độ cải thiện không bằng nhóm có sức co bóp bình thường. Do đó, DU không nên được coi là chống chỉ định tuyệt đối của phẫu thuật, nhưng cần thận trọng.
- Nomogram dự báo: Việc sử dụng các biểu đồ (nomograms) tích hợp nhiều thông số (IPSS, Qmax, PVR, thể tích tuyến) như mô hình của Hiệp hội Tiết niệu Châu Âu (EAU) hoặc các mô hình AI mới giúp tăng độ chính xác trong việc tiên lượng tắc nghẽn và khả năng phục hồi.
5. Quản lý Rối loạn Chức năng Tồn dư và Hướng đi Tương lai
5.1. Quản lý Biến chứng và Rối loạn Tồn dư
5.1.1. Bàng quang Tăng hoạt Tồn dư (Persistent OAB)
- Cơ chế: Do thay đổi thần kinh (denervation supersensitivity) hoặc thói quen bàng quang chưa kịp thích nghi.
- Điều trị:
- Dược lý: Thuốc kháng Muscarinic (Solifenacin) hoặc đồng vận Beta-3 (Mirabegron) có thể được khởi động sớm sau mổ. Nghiên cứu cho thấy chúng an toàn và hiệu quả, không làm tăng đáng kể nguy cơ bí tiểu ở bệnh nhân đã giải áp.
- PDE5 Inhibitors (Tadalafil): Sử dụng Tadalafil 5mg hàng ngày không chỉ hỗ trợ chức năng tình dục mà còn cải thiện triệu chứng OAB thông qua cơ chế tăng tưới máu vùng chậu và điều hòa tín hiệu NO/cGMP.
5.1.2. Thất bại khi rút ống thông (Failed TWOC) và Bàng quang Giảm hoạt (DU)
- Xử trí: Nếu bệnh nhân không tiểu được sau rút thông (TWOC thất bại), cần đánh giá lại bằng soi bàng quang để loại trừ tắc nghẽn cơ học (mảnh mô sót, máu cục). Nếu do DU, nên chuyển sang thông tiểu ngắt quãng sạch (CIC) thay vì lưu thông tiểu vĩnh viễn để giảm nhiễm trùng và duy trì độ đàn hồi bàng quang.
- Phác đồ: Sử dụng Alpha-blocker trước khi rút thông và thực hiện rút thông vào buổi sáng sớm (midnight removal) có thể tăng tỷ lệ thành công.
5.1.3. Tiểu không tự chủ (Incontinence)
- Thường là tạm thời (stress incontinence hoặc urge incontinence). Bài tập sàn chậu (Kegel) được khuyến cáo thực hiện sớm ngay sau khi rút thông để tăng cường cơ thắt ngoài và hỗ trợ kiểm soát bàng quang.
5.2. Các Liệu pháp Mới và Tương lai (Regenerative Medicine)
Đối với những bệnh nhân có bàng quang mất bù (end-stage bladder) hoặc DU nặng không hồi phục, y học tái tạo đang mở ra những hướng đi mới đầy hứa hẹn.
5.2.1. Liệu pháp Chống Oxy hóa và Kháng viêm
- Việc bổ sung các chất chống oxy hóa mạnh (như Eviprostat hoặc các hợp chất phytotherapeutic) trong giai đoạn chu phẫu có thể giúp giảm thiểu tổn thương I/R và ngăn chặn tiến trình xơ hóa. Nghiên cứu trên chuột cho thấy Eviprostat giảm stress oxy hóa và viêm, bảo vệ chức năng co bóp.
5.2.2. Liệu pháp Tế bào gốc (Stem Cell Therapy)
- Sử dụng tế bào gốc trung mô từ mô mỡ (ADSCs) hoặc tủy xương (BM-MSCs) tiêm trực tiếp vào thành bàng quang.
- Cơ chế: Tế bào gốc không chỉ biệt hóa thành tế bào cơ trơn mới mà quan trọng hơn là tiết ra các yếu tố tăng trưởng (paracrine effect) giúp tăng sinh mạch máu, bảo vệ thần kinh và điều biến miễn dịch, giảm xơ hóa.
- Thử nghiệm: Các kết quả sơ bộ trên người và linh trưởng cho thấy sự cải thiện về dung tích bàng quang và giảm PVR ở bệnh nhân DU.
5.2.3. Liệu pháp Gen (Gene Therapy)
- Chuyển gen mã hóa kênh Kali lớn (Maxi-K channels) (ví dụ: liệu pháp URO-902) đang được nghiên cứu để điều trị bàng quang tăng hoạt. Việc tăng biểu hiện kênh K+ giúp gây ưu phân cực màng tế bào, giảm tính hưng phấn quá mức của cơ chóp, từ đó giảm các cơn co thắt không tự chủ.
6. Kết luận
Sự phục hồi chức năng bàng quang sau phẫu thuật giải tắc nghẽn tuyến tiền liệt là một quá trình đa chiều, chịu ảnh hưởng bởi mức độ tổn thương phân tử trước đó và chất lượng của can thiệp phẫu thuật.
- Tính Khả hồi: Bàng quang có khả năng dẻo dai (plasticity) đáng kinh ngạc. Việc giải áp kịp thời có thể đảo ngược phì đại, giảm stress oxy hóa và cải thiện chức năng tống xuất. Tuy nhiên, xơ hóa mô kẽ lan rộng và mất phân bố thần kinh là những giới hạn của sự phục hồi.
- Vai trò của Phẫu thuật: Các kỹ thuật hiện đại như HoLEP/ThuLEP giúp tối ưu hóa kết quả phục hồi thông qua việc giải áp triệt để và giảm thiểu tổn thương mô lân cận.
- Cá thể hóa Điều trị: Việc sử dụng các công cụ tiên lượng (DWT, BCI, BOOI) cho phép phân tầng bệnh nhân, từ đó đưa ra chiến lược quản lý kỳ vọng và điều trị bổ trợ phù hợp (thuốc OAB, CIC, phục hồi chức năng) cho những trường hợp phục hồi không hoàn toàn.
- Tương lai: Y học tái tạo với liệu pháp tế bào gốc và gen hứa hẹn sẽ mang lại giải pháp cho những “bàng quang suy kiệt” mà phẫu thuật giải áp đơn thuần không thể cứu vãn.
Việc nhìn nhận phẫu thuật BPH không chỉ là “cắt bỏ tắc nghẽn” mà là “phục hồi chức năng hệ tiết niệu” là bước chuyển mình quan trọng trong tư duy lâm sàng của bác sĩ tiết niệu hiện đại.
Phụ lục: Bảng Dữ liệu Tổng hợp
Bảng 1: So sánh Tác động Phục hồi Chức năng giữa các Phương pháp Phẫu thuật
| Đặc điểm | TURP (Tiêu chuẩn vàng) | HoLEP / ThuLEP (Bóc nhân Laser) | GreenLight PVP (Bốc hơi quang) |
| Cơ chế giải áp | Cắt mô từng mảnh (Resection) | Bóc trọn thùy tuyến (Enucleation) | Làm bay hơi mô (Vaporization) |
| Mức độ giảm PVR | Tốt (+++) | Rất tốt (++++ – tương đương mổ mở) | Tốt (+++) |
| Cải thiện Qmax | Tốt (+++) | Rất tốt (++++) | Tốt (+++) |
| Phục hồi Triệu chứng (IPSS) | Ổn định dài hạn | Ổn định dài hạn | Ổn định, nhưng chậm trong 1-3 tháng đầu |
| Triệu chứng kích thích sau mổ | Trung bình (do vảy thương hàn) | Thấp (với ThuLEP), Trung bình (HoLEP) | Cao (do hoại tử đông sâu) |
| Thời gian lưu thông tiểu | 2-3 ngày | < 24 giờ – 1 ngày | < 24 giờ |
| Tỷ lệ tái can thiệp dài hạn | ~10-15% sau 10 năm | < 5% sau 10 năm | Có thể cao hơn HoLEP |
| Phù hợp tuyến lớn (>80g) | Hạn chế (nguy cơ TURS) | Rất phù hợp (Tiêu chuẩn mới) | Phù hợp, nhưng tốn thời gian |
Nguồn tổng hợp:
Bảng 2: Các Yếu tố Tiên lượng Phục hồi Chức năng Bàng quang
| Yếu tố | Chỉ số / Ngưỡng | Ý nghĩa Tiên lượng |
| Độ dày thành bàng quang (DWT) | > 2 mm (trước mổ) | Gợi ý tắc nghẽn rõ. Giảm sau mổ = Phục hồi tốt. Không giảm = Xơ hóa/Viêm. |
| Chỉ số Tắc nghẽn (BOOI) | > 40 | Tỷ lệ thành công cao. Tắc nghẽn là nguyên nhân chính. |
| Chỉ số Co bóp (BCI) | < 100 (DU) | Nguy cơ tồn dư nước tiểu sau mổ, nhưng vẫn có thể cải thiện nếu giải áp tốt. |
| Tuổi bệnh nhân | > 75-80 tuổi | Khả năng phục hồi trương lực cơ và thần kinh kém hơn. |
| Dung tích bàng quang | Nhỏ (Low compliance) | Tiên lượng xấu cho chức năng chứa đựng, nguy cơ suy thận. |
| Độ dài niệu đạo màng (MUL) | > 14 mm | Hồi phục tự chủ tiểu tiện nhanh hơn. |